近日,全国第一张干细胞 《药品生产许可证》 核发的消息,在业内引发轰动。消息传出后,A 股干细胞疗法概念股集体大涨,但短暂冲高后即齐齐跌落。根据北京药监局网站 「行政许可信息」 查询结果显示,铂生卓越生物科技 (北京) 有限公司 (以下简称 「铂生卓越」) 成为首家获得全国干细胞药品生产许可证的公司,这意味着该公司已具备生产干细胞药品的法定资格与能力。
公开信息显示,干细胞疗法与免疫细胞疗法是细胞疗法的两大分支,但与免疫细胞疗法近年来接连有天价产品获批上市的情况不同,干细胞疗法常常 「隐身」,后者更多关注点在于行业乱象、夸大宣传等负面标签。
其实在政策层面,中国已经明确提出要发展干细胞治疗等新技,并加快相关技术产品转化和临床应用,国家药品监督管理局 (CDE) 也发布了多项指导原则。与此同时,在产业方面已有一批研发 「正规军」 深耕该领域。
随着干细胞 「首证」 的核发,中国干细胞药物进入新阶段,具备了入市的基本条件。而且,此次获证的铂生卓越有一款干细胞药物已在今年 6 月被列入优先审批名单。
天顺财经 App 注意到,日韩等地已有多款干细胞疗法作为药品获批上市,但在全球认证最为严格的美国,FDA 至今尚未向任何干细胞药物出具 「通行证」。
「首证」 核发背后,干细胞药物陡然提速
在干细胞药物领域,目前全球有 11 款干细胞疗法作为药品获批上市,其中韩国 5 款、欧盟 2 款、日本 2 款,适应症涵盖皮下组织缺损、急性心肌梗死、克罗恩病等。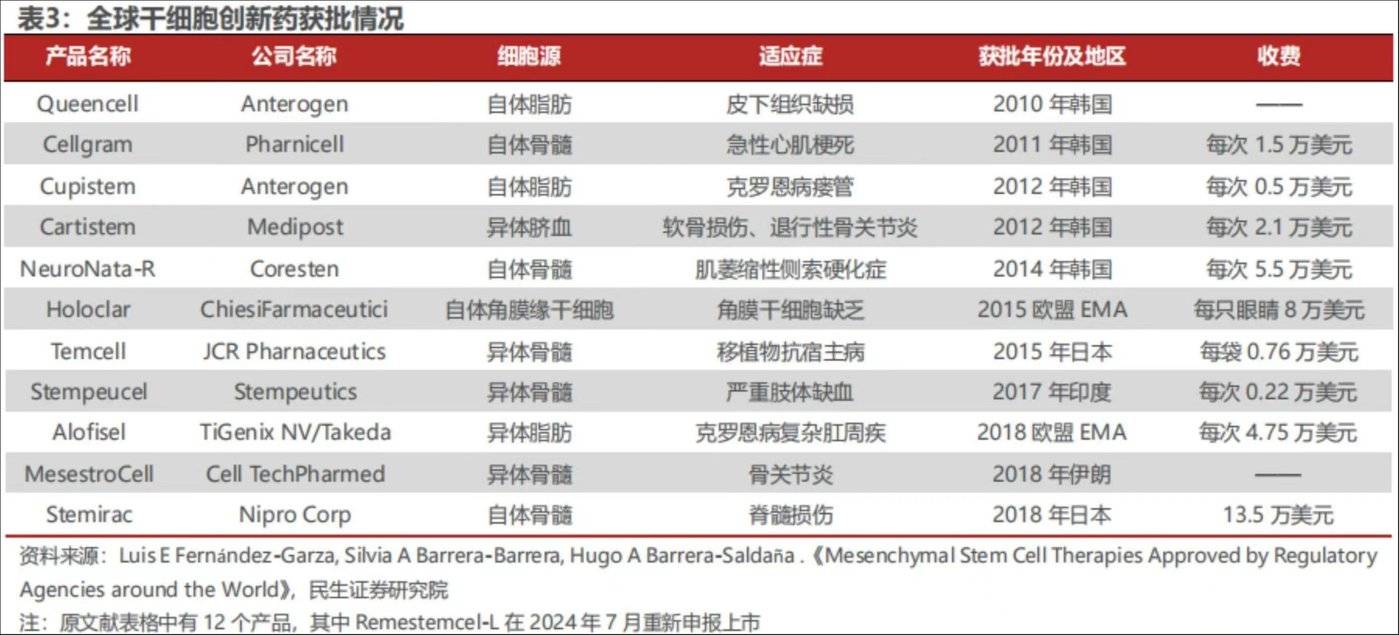
图源自民生证券研报
中美尚未有干细胞药品获批,但似乎只差临门一脚。
在中国,第一张干细胞 《药品生产许可证》 核发之前,首款干细胞药物也进入冲刺阶段。
2017 年开始,中国药品评价中心 (CDE) 逐步开始受理干细胞药物的临床试验申请,时隔 7 年,在今年 6 月 27 日,中国国家药品监督管理局药品审评中心公开信息显示,铂生卓越自主研发的 「艾米迈托赛注射液」(人脐带间充质干细胞),成为全国首款获得 NMPA 新药上市申请正式受理并纳入优先审评品种的干细胞新药 (受理号:CXSS2400062)。
数据显示,获得优先审评审批的药物上市注册申请的审评时限由常规程序的 200 日缩短至 130 日,获批速度显著提升。也就是说如果一切顺利,该款干细胞药物有望于今年获批,拿下 「1 号位」。
另外需要说明的是,间充质干细胞是一类多能干细胞,可从组织中分离获得并在体外培养和扩增,具有增殖能力强、分化潜力广泛等优点,在当前临床应用中最多。艾米迈托赛注射液就是人脐带间充质干细胞,其申请的临床适应症为激素失败的急性移植物抗宿主病 (aGVHD)。
约有 50% 的患者在接受同种异体骨髓移植 (BMT) 后会出现多系统损害的全身性疾病,即移植物抗宿主病 (GVHD),这也是造成患者死亡的重要原因之一。GVHD 分为急性 (aG) 和慢性 (cG),急性在骨髓移植后 3 个月内发病,在最严重的 aGVHD 患者中,尽管接受最佳疗法治疗,患者死亡率仍高达 90%。
而干细胞疗法在 GVHD 上的应用时间也比较长。
早在 2005 年,Osiris Therapeutics 开发的干细胞药物 Prochymal 被美国 FDA 授予孤儿药资格,适应症正是 GVHD。2013 年,Prochymal 被转让给澳大利亚公司 Mesoblast,并更名为 Ryoncil,又在 2015 年以 Temcell 的新商品名在日本获批,用于治疗 aGVHD,售价为 1 袋 86 万日元 (约 5 万人民币),每个疗程 8 袋。
今年 7 月,美国 FDA 接受 Mesoblast 旗下细胞疗法 Ryoncil(Remestemcel-L) 的生物制品许可申请提交,用于治疗类固醇难治性急性移植物抗宿主病 (SR-aGVHD) 儿童,该申请的 PDUFA 日期为 2025 年 1 月 7 日。
换言之,Ryoncil 有望成为美国首个同种异体 「现货型」 细胞疗法,而这也是该产品第三次寻求 FDA 获批。
干细胞药物获批进度加快的消息不断,国内相关概念股都有哪些?在干细胞药物领域的布局如何?当前国内的干细胞行业主要以什么业务为重?
概念股沸腾后速冻,干细胞产业格局待变
9 月份的第一个交易日,伴随着前述 「首证」 核发的喜讯,干细胞概念走强,中源协和(600645.SH)、南华生物(000504.SZ)、冠昊生物(300238.SZ) 纷纷涨停,但次日就全数收绿,回吐大部分涨幅。
热门概念 「一日游」 在 A 股并不罕见,就干细胞药物来说,虽然有望迎来新突破,但大部分管线距离商业化仍然遥远,进入临床 III 期的阶段的都数目寥寥。
据民生证券不完全统计数据结果,获批 CDE 临床试验默示许可的约 89 个干细胞新药中,处于 III 期临床试验仅约 3 项,II 期临床试验约 10 项,适应症涉及关节、肺及呼吸疾病、抗宿主病、肝衰竭肝硬化、肛肠、脑卒中等多种疾病。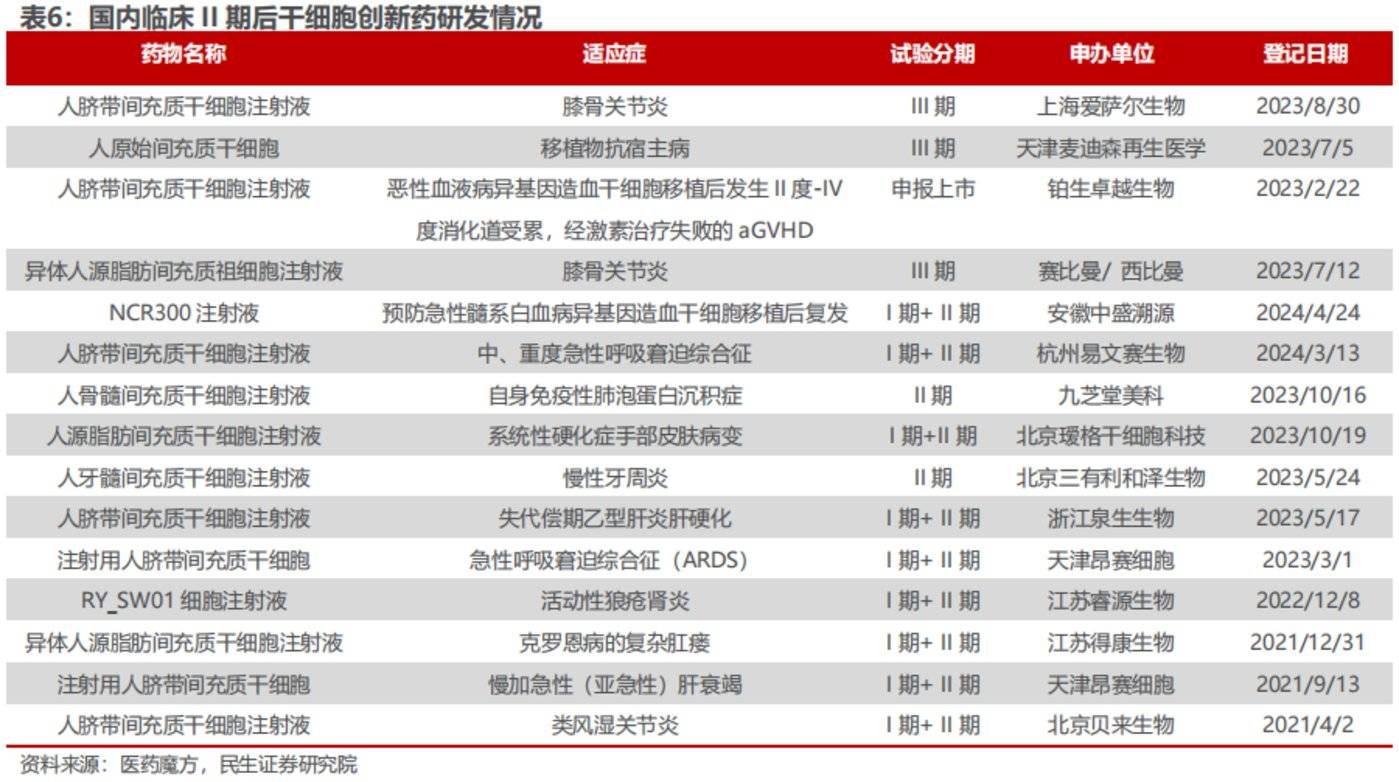
图源自民生证券研报
在干细胞产业,上游的干细胞提取与存储是基础的前端业务,资本聚集最多;中游是干细胞产品化,主要攒聚着干细胞增殖与药物研发企业,主要从事技术研发工作,囊括干细胞增殖、干细胞药物研发、实验室处理配套产品 (如检测试剂) 等;下游是应用市场,包括开展干细胞治疗临床研究及应用的医疗机构,以及一些医疗美容服务机构。
相较于干细胞药物的竞速赛,行业主要的竞争仍在产业上游的干细胞存储赛道。干细胞存储是指将干细胞于不同人体组织中分离培养,再经检测鉴定后冻存于-196℃的深低温,未来有临床需求时,可将干细胞复苏后回输给患者,以治疗疾病。
干细胞存储是 「牌照生意」,也是干细胞行业最成熟的产业化项目。在 A 股市场,仅中源协和、南京新百(600682.SH) 拥有造血干细胞库牌照,分别有四张 (山东、北京、浙江、广东) 和一张 (天津),另外有两张牌照在铸信集团、聚康生物旗下。
目前,国内的干细胞存储主要是自新生儿脐带血中提取造血干细胞,随着新生儿出生数量的下滑,存储业务面临挑战,行业向中游的干细胞产品延伸是大势所趋,但这也是一个投入高、周期长的领域。
以百货商店起家的南京新百拥有世界最大的脐带血干细胞存储应用平台,但在干细胞药物方面涉猎不多,公司通过收购丹瑞美国,布局了免疫细胞治疗药物。
中源协和近年来将业务向干细胞药物领域延伸,其参股的北京三有利和泽生物与首都医科大学共同申报的 「人牙髓间充质干细胞注射液」 治疗慢性牙周炎已于 2023 年 5 月开始 II 期临床。其全资子公司武汉光谷中源自主研发的 VUM02 注射液 (人脐带源间充质干细胞注射液) 已有六个适应症申报临床。
除此之外,在 A 股的干细胞概念中,关注度较高的南华生物、冠昊生物、戴维医疗(300314.SZ)、泰林生物(300813.SZ)、开能健康(300272.SZ)、我武生物(300357.SZ)、济民健康(60322.SH) 等个股中,业务落脚点多在干细胞产业的上游领域。
值得一说的是,南华生物的人脐带间充质干细胞注射液在今年获中检院权威质量认证;我武生物此前在投资者问答表中,在研的干细胞治疗药物处在临床前研究阶段;济民健康 2024 年半年报显示,其研发项目中包括各种类型的干细胞治疗技术,涉及视网膜色素变性、2 型糖尿病、前列腺癌等多种疾病的治疗。
(本文首发于天顺财经 App 作者丨杨亚茹 编辑丨曹晟源)
